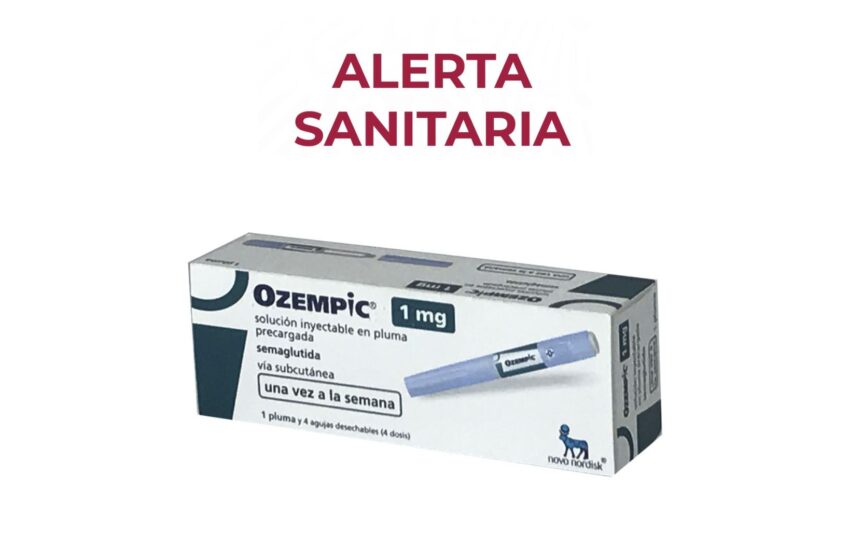
La Comisión Federal para la Protección contra Riesgos Sanitarios (Cofepris) emitió una alerta sanitaria luego de detectar la falsificación del medicamento Ozempic 1mg (semaglutida), en su presentación de solución inyectable en pluma precargada.
La alerta se derivó después de que la empresa importadora Novo Nordisk México detectara un lote falsificado en circulación en territorio nacional.
El producto apócrifo corresponde al lote LP1F832, que cuenta con la fecha de caducidad de 31/10/2026. La autoridad sanitaria señaló que dicho lote cuenta con múltiples anomalías que lo vuelven peligroso para los consumidores.
De acuerdo con el análisis técnico-documental, el producto falsificado no contiene el principio activo (semaglutida), el cual proporciona su efecto terapéutico.
Asimismo, la pluma precargada ha sido reetiquetada y no corresponde al producto original, ya que los textos y leyendas están escritos en un idioma diferente al español. Además, los números de lote no coinciden entre en envase secundario y la pluma precargada.
“Representa un riesgo para la salud de la población, ya que se desconoce su procedencia, condiciones de fabricación, almacenamiento, distribución y transporte, así como las materias primas empleadas en su elaboración”.
Cofepris.
Ozempic es un medicamento que requiere receta médica para su adquisición, ya que su uso indiscriminado y sin supervisión médica puede representar un riesgo.
Recomendaciones para la población y profesionales de la salud:
- Realizar una verificación visual de los empaques antes de usar cualquier medicamento. Corroborar que los números de lote y fechas de caducidad coincidan, y que la pluma no tenga rastros de manipulación o alteración.
- No comprar medicamentos en plataformas de comercio electrónico, sitios web, aplicaciones móviles, vía pública, tianguis o establecimientos informales, especialmente los que requieren receta médica.
- Si se detecta el producto con las anomalías descritas, no comprarlo ni utilizarlo. En caso de haberlo usado, suspenda de inmediato su uso y consulte a un profesional de la salud.
La Cofepris invita a la población a denunciar cualquier información sobre la comercialización del producto falsificado mediante el siguiente enlace: Denuncia Sanitaria.
También puedes leer: SAT lanza programa para eliminar multas y recargos; ve de qué se trata